随着微创与美观需求的持续增长,免缝闭合技术在医疗器械领域正逐步替代传统针线缝合。本文从合规基础、临床价值、技术迁移路径与生产保障四个维度,解析解剖免缝闭合技术的迁移逻辑,为品牌方提供高效、合规的OEM/ODM合作路径。
康丽达一次性使用免缝闭合器(注册证号:苏械注准20222022028)已通过江苏省药品监督管理局审批,核心参数可供品牌方直接复用,大幅降低技术迁移的合规成本。
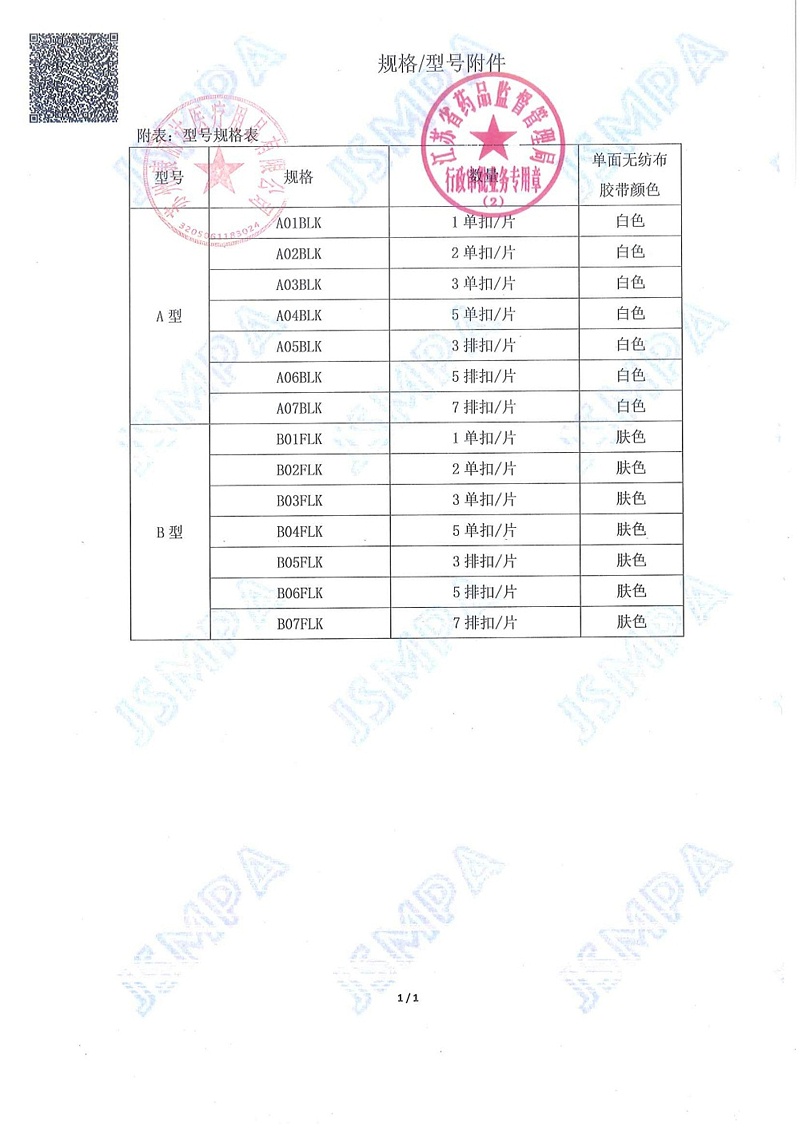
结构组成:聚丙烯(PP)拉扣组件、医用压敏胶带(透气无纺布基底)、离型纸(环氧乙烷灭菌保障无菌)
适用范围:用于体表各部位伤口的闭合,避免传统针线缝合带来的穿刺损伤
该产品结构清晰、参数明确,为品牌方在合规框架内进行二次开发提供了高起点。

对照组(针线缝合):平均针眼瘢痕数 3.2个/cm
试验组(免缝闭合器):针眼瘢痕数 0个/cm
机制解析:通过医用胶带与自锁器实现皮肤减张闭合,避免针线穿透真皮层,从源头消除针眼瘢痕,满足医美与精细化愈后需求。
缝合时间缩短58%:传统缝合12.3分钟 → 免缝闭合5.2分钟
护士培训周期压缩:从2周缩短至2天,操作标准化显著提升临床流转效率
在合规框架下,品牌方可直接复用已注册的核心参数,如胶带粘性、拉扣力学性能、灭菌工艺等,减少重复验证工作。
某医美品牌希望开发透明款免缝闭合器,以提升美观性。康丽达提供以下解决方案:
复用参数:胶带粘性参数(0.086N/cm)
替换材料:将无纺布基底替换为医用聚氨酯透明膜
开发周期:3个月完成变更注册,复用原注册证90%数据,显著缩短上市时间
康丽达严格执行医疗器械生产质量管理规范,确保每一批次产品稳定合规:
生产环境:10万级洁净车间(GMP认证号:苏药监械生产许20220338)
质控体系:
万级生物实验室(微生物检测)
物理实验室(拉力测试仪实时监控)
本产品用于闭合已止血的清洁伤口,不适用于感染创面、活动性出血伤口。
对聚丙烯或医用压敏胶过敏者禁用。
免缝闭合器:苏械注准20222022028
自粘敷料:苏械注准20222142033

结语
解剖免缝闭合技术的迁移,不仅是产品的迭代,更是从合规、临床到生产体系的系统升级。康丽达以成熟的注册基础、灵活的定制能力与严苛的生产标准,助力品牌方高效完成技术迁移,抢占微创闭合赛道先机。
了解更多医疗器械代工合作方案,欢迎联系我们。